皮膚科学研究における包括的技術基盤
トランスレーショナル・プラットフォーム
皮膚科学研究イノベーション

補完的技術基盤
TNOではヒト皮膚科学における最先端かつ包括的な研究プラットフォームを提供しています。
その専門性はR&Dの全領域を網羅しており、計算科学に基づいた安全で持続可能な設計(Safety & Sastainablility by Design)、前臨床試験用のin vitro皮膚モデル、高解像度な分子解析およびマルチオミクス解析、in vivo臨床研究、そして持続的な皮膚モニタリングを可能にするウェアラブル技術まで多岐にわたります。
これらの機能は、単独での活用はもちろん、目的に応じて最適に組み合わせて展開することが可能です。
幅広い応用領域
TNOは、多国籍企業から公的機関に至るまで、多角的なパートナーシップを通じて皮膚科学領域のイノベーションを加速させています。
個別のテーラーメイド型コンサルティングや調査研究から、共同イノベーションの推進、さらにはマルチステークホルダーによるイニシアチブのオーケストレーション(調整・統括)まで、幅広く対応します。
産官学連携の推進
本研究プラットフォームを通じて、製薬および化粧品業界のパートナー企業へ、皮膚の健康におけるブレイクスルーを創出するための統合的・科学主導型・将来を見据えたアプローチを提供します。
最先端技術と広範な多角的専門知識、そして独立した検証機能を融合させることで、組織の開発リスクを低減し、エビデンスを強化するとともに、安全で効果的かつ持続可能なイノベーションの迅速な市場投入を支援します。
パートナーと共に、個人、産業、社会のための次世代スキンヘルス・ソリューションを形作っていきます。
ヒト 3D 皮膚モデルによる生理学的評価プラットフォーム
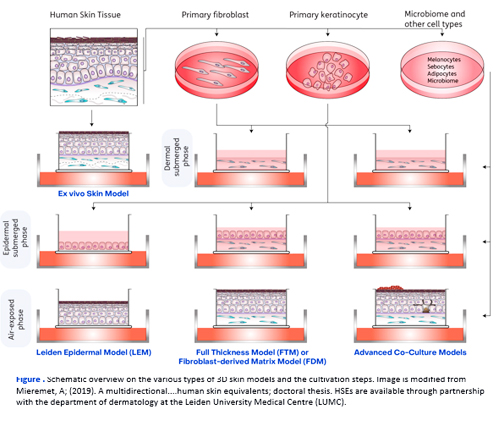
ヒト 3D 皮膚モデルを活用することで、生理学的に妥当な環境下での介入効果の検証が可能となります。研究プロジェクトに求められるスループットや複雑性に応じて、多種多様な 3D モデルを構築・展開しています。
Ex vivo Skin Model
Ex vivo Skin Modelは、形成外科手術(美容整形等)によって得られた生検組織の培養に基づいています。本モデルにおける細胞組織構造および細胞外マトリックス(ECM)は、ヒト生体内の皮膚を極めて忠実に反映しています。
ヒト培養皮膚モデル(HSE: Human Skin Equivalents) :
● Leiden Epidermal Model (LEM)
LEM は、ヒト初代培養角化細胞(Primary keratinocytes)を培養し、表皮構造を再構築したモデルです。浸漬培養期(Submerged phase)において角化細胞が増殖しインサート全面を被覆した後、気液界面培養期(Air-liquid interface phase)において分化が誘導されます。
終末分化を経て、LEM は主要なすべての表皮分化層を形成します。本モデルは、ハイスループットスクリーニング(HTS)へのスケールアップが可能です。
● Full Thickness Model (FTM)
FTM は、線維芽細胞と角化細胞の両方で構成される 3D 皮膚モデルです。
線維芽細胞をコラーゲンマトリックス内で培養することで皮膚の真皮コンパートメントを模倣しており、両細胞種が共存しているため、線維芽細胞と角化細胞の相互作用(Crosstalk)を評価することが可能です。
● Fibroblast-Derived Matrix Model (FDM)
FDM も同様に、皮膚の主要な 2 種類の細胞を用います。FDM の特徴は、線維芽細胞自身が細胞外マトリックスを分泌・再構成する点にあり、マトリックスは完全に細胞由来のタンパク質のみで構成されます。
特定の線維芽細胞サブタイプを用いることで、より深層の真皮層を反映させることも可能です。
Advanced Co-Culture Models
高度な共培養モデルにより、さらに複雑な病態の再現が可能です。メラノサイト(色素細胞)、皮脂細胞、または脂肪細胞といった追加の細胞種を導入できます。ホスト-マイクロバイオーム(常在菌叢)相互作用を評価するために、細菌、ウイルス、または真菌の局所適用(Topical application)も実施可能です。
次世代の高度モデルには、免疫応答能保持(Immunocompetent)モデルやSkin-on-a-chip(生体模倣システム)も含まれます。
皮膚マイクロバイオーム(Skin Microbiome)研究プラットフォーム
皮膚マイクロバイオームは、皮膚表面に生息する細菌、真菌、ウイルス、およびダニ(ヒゼンダニ等)から構成される多様な微生物コミュニティです。これは、有害な病原体に対する防御機能や皮膚免疫機能の維持において極めて重要な役割を担っています。
マイクロバイオームの恒常性が保たれている状態は皮膚の健康に寄与しますが、その攪乱(ディスバイオーシス)は、ざ瘡(ニキビ)や湿疹(アトピー性皮膚炎等)といった皮膚疾患の一因となります。
 菌株の収集と培養(Strain collecting and culturing)
菌株の収集と培養(Strain collecting and culturing)
皮膚マイクロバイオーム菌株収集プロセスは、健常または疾患皮膚から代表的な微生物を分離し、単離株としての解析を可能にすることを目的としています。
培養により、個々の菌株の増殖特性や表現型解析(Phenotypic study)が可能となります。
自社内で実施する全ゲノム解析(Whole-genome sequencing: WGS)により、これらの菌株を高解像度で特性解析し、分類学的位置付け、機能遺伝子、および菌株レベルの多様性を明らかにします。
収集された菌株は、宿主関連メタデータと統合された形でTNO菌株コレクションに保存され、研究開発プロジェクトにおいて利用可能です。。
皮膚マイクロバイオームの特性評価(Characterization)
皮膚マイクロバイオームを複雑なエコシステムとして解析・評価することは、皮膚の健康との相関を理解する上で不可欠です。我々は、マイクロバイオーム評価のための高度な手法を複数確立しています。
● ホストDNA除去スワブ法: サンプル中のヒト由来DNAの混入を低減し、微生物由来DNAを効率的に濃縮・抽出します。
● 16S rRNA遺伝子メタゲノム解析: 属または種レベルでの細菌叢構成および相対存在量をプロファイリングします。
● ショットガンメタゲノミクス: 高精度な分類学的同定に加え、微生物が保有する遺伝子や代謝経路の直接的な評価を可能にします。
統合的なバイオインフォマティクス解析により、各サンプルの分類学的特性(Taxonomy)と機能的ポテンシャル(Functional capacity)の双方を明らかにします。
In vitro 皮膚マイクロバイオームアッセイ
In vitro マイクロバイオームアッセイでは、定義された菌叢(Defined bacterial communities)を用いることで、制御された条件下で微生物間の相互作用をモデル化します。
これにより、細菌の増殖、競合、および栄養素や化合物といった外的要因に対する応答を詳細に検討することが可能です。
当社のテーラーメイド型アッセイは、in vivo 系の複雑性を排除しつつ、マイクロバイオームの動態に関する再現性の高い知見を提供します。
菌株エンジニアリング(Strain engineering)
皮膚常在菌のエンジニアリングでは、本来の皮膚常在菌を改変し、抗菌物質の産生能強化やバリア機能のサポートといった有益な機能を付与・増強します。
これらの改変株については、安全性、安定性、およびホスト適合性を最優先に考慮しつつ、医薬品および化粧品への応用展開を探索しています。
ホスト-微生物相互作用モデル(Host-Microbe Interaction Models)
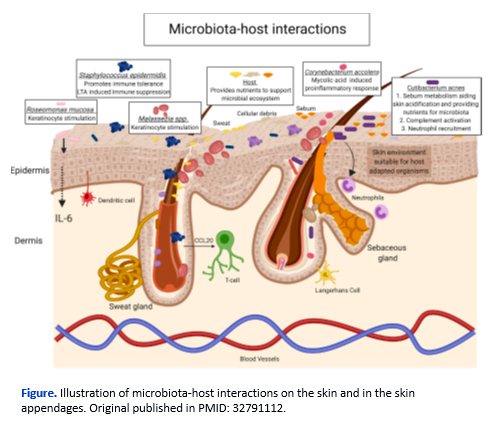
マイクロバイオームとヒトホストとの相互作用の解明には、共培養モデルが不可欠です。TNOでは、科学研究において幅広く適用可能な多種多様なホスト-微生物相互作用モデルを開発してきました。
これには、細菌、真菌、および/またはウイルスを導入した初代細胞(Primary cells)ベースの 2D モデルが含まれます。
さらに、皮膚における生理学的に妥当な相互作用の検証には 3D モデルが用いられ、単一培養、または混合培養によるマイクロバイオームの再構成・強化が可能です。
2D 細胞-微生物アッセイによるスクリーニング
皮膚ホスト-微生物相互作用モデルでは、角化細胞(ケラチノサイト)、線維芽細胞、またはその他の皮膚細胞種の 2D 培養系をヒトホストの代表として使用します。
これらのモデルを細菌、真菌、またはウイルスと共培養することで、皮膚細胞に対する微生物の直接的な相互作用を研究できます。
これにより、免疫応答、バリア機能、および皮膚生理に対する微生物の影響を、制御された環境下で詳細に調査することが可能となります。
3D ホスト-微生物共培養モデルによる検証
再構築表皮(RhE)や全層皮膚モデル(FTM)を含む 3D 皮膚モデルは、組織構造およびバリア機能をより忠実に再現(Recapitulate)します。
これらのシステムは、成層化した環境(Stratified context)内に複数のホスト細胞種を包含しており、生理学的に妥当なホスト-微生物相互作用を可能にします。
細菌、真菌、またはウイルスを定着(Colonization)させることで、空間的な組織化やニッチ特異的(Niche-specific)な微生物動態の調査が可能となります。
3D モデルは、2D 培養では評価が困難な複雑な免疫応答や代謝応答を捉えることができるため、皮膚生物学、疾患メカニズム、およびマイクロバイオーム標的介入の研究におけるトランスレーショナル・プラットフォームとして機能します。
アトピー性皮膚炎およびざ瘡(ニキビ)に対するテーラーメイド・アプローチ
3D ホスト-微生物共培養モデルをモジュレートすることで、特定の皮膚構造やバリア欠陥を組み込み、アトピー性皮膚炎(AD)やざ瘡(アクネ)に特異的な疾患解析が可能となります。
黄色ブドウ球菌(Staphylococcus aureus)やフィロタイプ特異的なアクネ菌(Cutibacterium acnes)などのパソビオン(Pathobionts:潜在的病原体)を選択的に定着させることで、疾患に関連する微生物動態を再現します。
これらのモデルは、炎症、ホストの感受性、およびマイクロバイオーム標的介入に関するメカニズム解析やトランスレーショナル研究を促進します。
Publication
Scientific Reports. March 2026
Advancing human skin models by integrating skin microbes for next-generation research.
Tissue Engineering Part A. Dec 2017
Recapitulation of Native Dermal Tissue in a Full-Thickness Human Skin Model Using Human Collagens.
Eur J Dermato. June 2017
Differential effect of extracellular matrix derived from papillary and reticular fibroblasts on epidermal development in vitro.
Mutagenesis. Mar 2011
Development and characterisation of an in vitro photomicronucleus test using ex vivo human skin tissue.
Toxicology in vitro. Aug 2008
Leiden reconstructed human epidermal model as a tool for the evaluation of the skin corrosion and irritation potential according to the ECVAM guidelines.

