家族性高コレステロール血症・動脈硬化症マウスモデル
ApoE*3Leiden・ApoE*3Leiden. hCETP mouse, model for Atherosclerosis, Familial hypercholesterolemia
ApoE*3Leiden、ApoE*3Leiden. hCETP transgenic mouse.
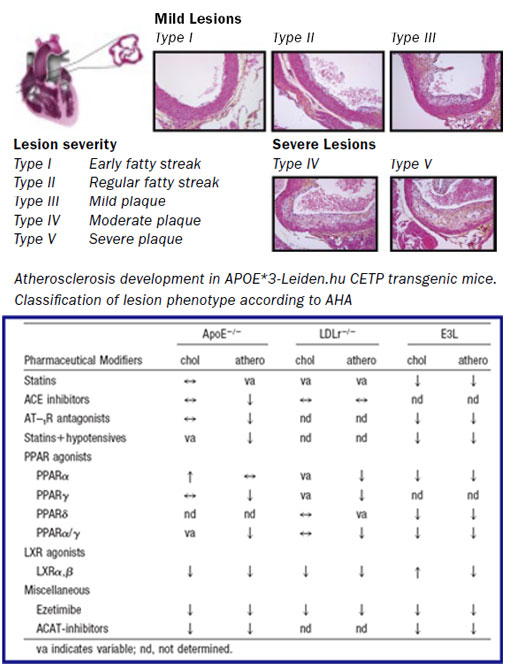
APOE*3-Leiden:脂質代謝および動脈硬化研究のトランスレーショナルモデル
本トランスジェニックマウス系統は、ヒト apoE*3-Leiden および apoc1 遺伝子の導入により作出されました。優性変異である E*3-Leiden 変異の主要な表現型は、LDL受容体(LDLR)に対する親和性低下に起因する、トリグリセリド(TG)リッチリポタンパク質(カイロミクロンおよびVLDLレムナント)のクリアランス不全です。一方、APOC1の過剰発現はリポリシス(脂質分解)を阻害します。
野生型(WT)マウスが apoB 含有リポタンパク質を極めて迅速に消失させるのに対し、E3L マウスはクリアランス遅延を示し、ヒトにおける代謝動態をフェノコピー(模倣)しています。その結果、E3L マウスは家族性ジスベタリポタンパク血症(III型高脂血症)患者に類似したリポタンパク質プロファイル(血中コレステロールの大部分が (V)LDL 画分に存在)を呈し、飽和脂肪酸およびコレステロール負荷により動脈硬化病変を形成します。
ただし、E3L マウス(WTマウス同様)はヒトのリポタンパク質代謝に不可欠なコレステロールエステル転送蛋白遺伝子を欠損しているため、HDL調節薬に対する反応性は認められません。
APOE*3-Leiden.huCETP (E3L.CETP) マウス
本ダブルトランスジェニックマウスは、血漿脂質、動脈硬化、代謝症候群、および MASH肝線維症に対する薬物やバイオアクティブな食品成分の有効性評価において、極めて有用なモデルであることが立証されています。
本モデルは、TNO独自の APOE*3-Leidenマウスを基盤としています。
E3L.CETP マウスは、内因性プロモーター制御下にあるヒト CETPを導入することで、HDLから apoB 含有リポタンパク質へのコレステロールエステル転送(およびTGの逆転送)という、よりヒトに近いリポタンパク質代謝系を構築しています。
この催アテローム性リポタンパク質分布のシフトにより、E3L.CETP マウスはWTD負荷において、E3L マウスよりも高度な動脈硬化病変を呈します。
薬物反応性とトランスレーショナルな特徴
ApoE3L および ApoE3L.CETP マウスは、以下の優れた特性を有しています。
● 臨床薬への高い反応性: スタチン、フィブラート、ナイアシン、エゼチミブ、PCSK9 阻害抗体、ANGPTL3 阻害抗体など、既存の脂質異常症治療薬に対し、臨床用量に近似した用量でヒトと同様の反応を示します。
● 脂質プロファイルの滴定可能性: 食餌介入により、コレステロールおよび TG を所望のレベルに調整可能です。
● 柔軟な試験デザイン: 動脈硬化の進行(予防)および退縮(治療)の両デザインで実施可能です。
特に E3L.CETP マウスは、HDL および TG モジュレーターの評価に適しており、CETP 阻害薬等による apoB 含有リポタンパク質の低下と HDL の上昇が確認されています。
ApoE欠損LDL受容体欠損マウスとは異なり、E3L.(CETP) マウスは機能的な apoE-LDLR クリアランス経路を保持しているため、PCSK9 や ANGPTL3 阻害薬の介入研究に最適です。
アリロクマブやエビナクマブをスタチンに上乗せ投与した試験では、マウスモデルとして初めて動脈硬化病変の真の退縮(True regression)が報告されています(Pouwer et al. JLR 2020)。
臨床予測能とバイオ医薬品への応用
本モデルは、糖尿病性脂質異常症に類似した混合型脂質異常症の病態を呈し、臨床予測能の高いモデルとして知られています。例えば、臨床試験で不成功に終わった GPR109a アゴニスト(MK-0354)や CETP 阻害薬トルセトラピブ、特定の植物ステロール誘導体などは、本モデルにおいても有効性を示しませんでした。
バイオ医薬品研究においては、PCSK9、ANGPTL3、CETP、酸化LDL、内皮リパーゼ、IL-6 等を標的とした抗体、siRNA、miRNA、ASO、ワクチン、さらに GLP-1R アゴニスト等の評価に 200 以上のプロジェクトで利用されています。
非脂質標的および併用療法
本モデルは、抗炎症薬や降圧薬の有効性評価にも適しています。
● 抗酸化作用: Resolvin E1 (Salic et al. Atherosclerosis 2016); Epicatechin (Morrison et al. Atherosclerosis 2014); Quercetin (Kleemann et al. Atherosclerosis 2011); Salicylate (de Vries-van der Weij et al. Atherosclerosis 2010)などが、脂質低下作用とは独立して(あるいは相加的に)動脈硬化の進行を抑制することが示されています。
● 高圧薬: Calcium antagonist amlodipine (Trion et al. J Cardiovasc Pharmacol 2006, efficacy independently of BP-lowering in E3L), Angiotensin II receptor blocker Olmesartan (van der Hoorn et al. J Hypertension 2007, in E3L) Renin inhibitor aliskiren (Kuhnast et al. J Hypertension 2012, in E3L.CETP)などが、血中コレステロール値に影響を及ぼさずに病変を改善し、プラーク表現型を安定化させることが確認されています。
● スタチンの多面的作用(Pleiotropic effects): スタチンの抗炎症作用を、脂質低下作用と分離して評価した研究も実施されています。
管内皮機能障害の評価
MRI を用いた胸部・腹部大動脈の血管機能および大腿動脈の血流依存性血管拡張反応(FMD)の解析により、加齢に伴う内皮機能障害の評価が可能です。E-/-やLDLR-/-マウスと異なり、動脈硬化形成前段階における脂質異常および加齢の影響を独立して評価できる点が、本モデルのユニークな優位性です。
心血管安全性(Cardiovascular Safety)
脂質代謝、炎症、動脈硬化に対する高い感受性から、薬剤の副作用に起因する心血管リスクの検出に有用です。トルセトラピブや特定の抗腫瘍薬(ベキサロテン、チロシンキナーゼ阻害薬のイマチニブ、ニロチニブ、ポナチニブ等)の CV 安全性プロファイルの評価に活用されています。
技術資料ダウンロード:
□ Models for Cardiovasucular and Metabolic diseases (Brochure EN)
□ Cardiovasucular Safety (Brochure EN)
□ 発表論文リスト ver.Jan2026
□ Recent Publication:
New Modelity
Proof-of-concept study for liver-directed miQURE technology in a dyslipidemic mouse model. Molecular Therapy Nucleic Acids, June 2023
Regression study
Alirocumab, evinacumab, and atorvastatin triple therapy regresses plaque lesions and improves lesion composition in mice. Pouwer et al. JLR 2020:
Latest publication
□ Efficacy of a novel PCSK9 inhibitory peptide alone and with evinacumab in a mouse model of atherosclerosis.
J Lipid Res 2025; Inia JA, van Nieuwkoop-van Straalen A, Jukema JW, Rolin B, Staarup EM, Mogensen CK, Princen HMG, van den Hoek AM.
□ Obicetrapib and ezetimibe enhance LDL receptor-mediated VLDL-clearance and regress atherosclerosis on atorvastatin background.
J Lipid Res 2026 (conditionally accepted); Inia JA, Zhang L, Keijzer N, Worms N, van Nieuwkoop-van Straalen A, Ditmarsch M, de Kleer M, Jukema JW, Kastelein JJP, Szarek M, van den Hoek AM, Stokman G, Pieterman EJ, Princen HMG.
AI駆動型 前臨床動脈硬化研究:TNO Athero AI
APOE*3-Leiden (E3L) および APOE*3-Leiden.huCETP (E3L.CETP) マウスは、血漿脂質、リポタンパク質代謝、および動脈硬化を標的とした治療薬評価において確立されたトランスレーショナルモデルです。
これらのモデルは、予防および治療的試験デザインの双方において、臨床で使用される脂質低下薬に対する良好な反応性が証明されています。
AI支援型の評価は、病変(Lesion)定量の標準化、観察者間・内誤差(Inter- and Intra-reader variability)の低減、および薬効検出感度の向上により、これらの研究をさらに高度化します。
TNO Athero AI は、ルーチンの H&E 染色大動脈基部(Aortic root)切片画像を、客観的かつ定量的なデータセットへと変換し、薬効データの信頼性を強固なものにします。
 一貫性のあるスコアリング (Score with consistency)
一貫性のあるスコアリング (Score with consistency)
動脈硬化試験および研究におけるばらつきを最小限に抑えることで、スコアリングの信頼性を向上させます。
TNO Athero AI は、すべての病変を同一の客観的基準で評価することを保証し、人間の評価者間や異なる解析セッション間で生じる主観的な差異を排除します。
セグメンテーションと分類 (Segment and classify)
TNO Athero AI は、プラークを正確にセグメンテーション(領域分割)し、壊死層(Necrotic core)、石灰化、線維性組織、平滑筋成分などの組成を詳細に特徴付けます。
この詳細な組成解析により、従来の面積ベースの測定では完全に見逃されていた治療効果を明らかにすることが可能です。
ワークフローの効率化 (Efficient workflows)
AI支援型の読み取りにより、解析期間(ターンアラウンドタイム)を短縮し、試験を加速させます。
自動解析プロセスは、数百枚のホールスライド画像(WSI)を、病理医による手動レビューのわずかな時間で処理し、品質や詳細を損なうことなく迅速なデータ提供を可能にします。
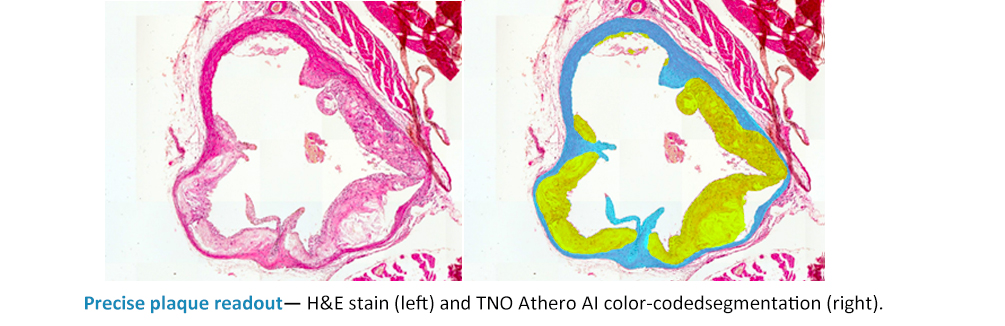
精密かつ標準化されたプラーク解析 (Precise and standardized plaque readout)
TNO Athero AI のセグメンテーション技術は、精密かつ標準化されたプラークのデータ読み取りを可能にし、大動脈基部横断切片全体にわたって病変境界を正確に画定(Delineation)します。
自動解析により解析期間を短縮し、評価者のばらつきを最小限に抑える一方、明確なカラーコード出力により、結果の解釈を容易にします。各プラーク構成要素はピクセルレベルの精度でマッピングされ、手動評価の限界を遥かに超える定量測定を提供します。
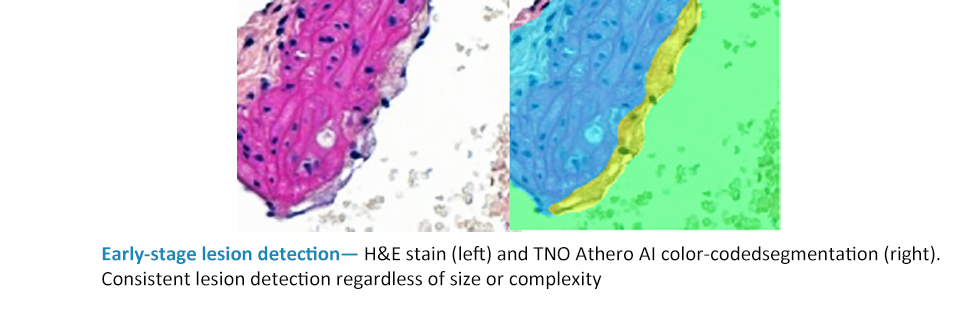
早期病変の安定した検出 (Consistent detection of early-stage lesions)
TNO Athero AI 解析は、すべての試験サンプルにおいて、微小な早期動脈硬化病変であっても一貫して検出・画定することを保証します。薬物介入によって病変負荷が大幅に減少する可能性がある「予防投与デザイン」の試験において、この検出感度は極めて重要です。
AI モデルは、特徴の見落としリスクを低減し、試験内および試験間での病変評価の信頼性を高め、わずかではあるが有意な治療効果を統計的確信をもって捉えることを可能にします。
HistoSuiteの解析期間について
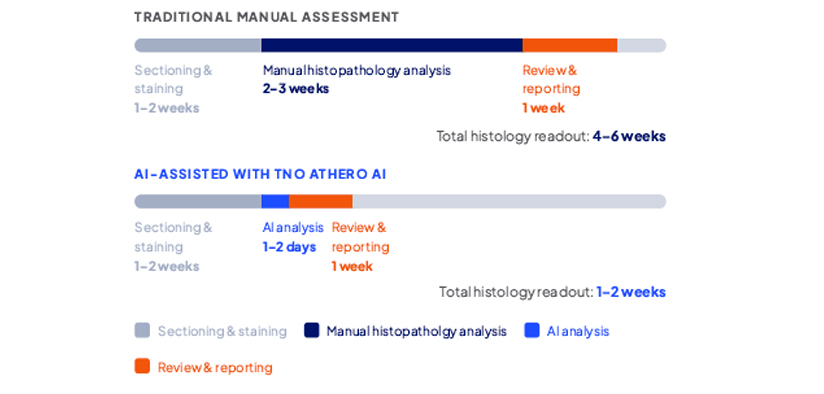 TNO Athero AI は、プラーク評価において最も労力を要する工程を自動化することで、深度、精度、再現性を犠牲にすることなく、解析期間を数週間から数日へと短縮します。
TNO Athero AI は、プラーク評価において最も労力を要する工程を自動化することで、深度、精度、再現性を犠牲にすることなく、解析期間を数週間から数日へと短縮します。

